多発性硬化症センター
国立病院機構宇多野病院 関西脳神経筋センターでは、
多発性硬化症センターを開設しています。
多発性硬化症(以下、MS)は、昭和47年から始まった我が国の難病対策の一つとして当初から取り組まれてきた神経難病であり、免疫性神経疾患の代表的な疾患です。50年以上に渡る多くの研究により、MSと異なる視神経脊髄炎(以下、NMOSD)が混在していることが判明し、この数年間で、両疾患の治療方法・治療薬において、目覚ましい進歩がとげられています。
当院は、我が国の診療ガイドラインにも積極的に参加し、2010年、2017年、そして2023年にMS・NMOSD診療ガイドライン2023(医学書院)が発行されています。日本神経学会監修の診療ガイドラインであり、当院臨床研究部(田原将行医師)も研究分担者として協力しています。当院が中心となり実施した医師治験治験(RIN-1試験)により承認されたリツキサン®(NMOSD治療薬)が、NMOSDの新たな治療薬として掲載されています。
2024年時点で、NMOSDは5種類の治療薬、MSは6種類の再発寛解型治療薬以外にも進行型治療薬2種類が登場しています。
両疾患とも再発が抑制可能な時代に突入しました。治療薬がない時代から、これらの治療を適切に使う時代に変わりました。
しかし、進行型MS治療は未だ十分でなく、再発寛解型から進行型へ進んでしまうリスクは完全に抑制できていません。
NMOSDにおいても、AQP4抗体陰性例の中から、MOGAD(MOG抗体関連疾患)という治療法が異なる疾患が出現しており、新たな挑戦を続けています。
受診の予約(平日9:00~17:00)は、当院地域医療連携室で行っています。
予約電話番号:075-461-5121
※神経免疫外来診察日(田原)は、月・木曜日 午前中 (予約制)になります。
プレスリリース
宇多野病院が中心となり全国8施設で実施した医師主導治験(RIN-1試験)の結果により、視神経脊髄炎(NMOSD)患者さんの新たな治療薬(リツキサン®️)が保険承認されました
抗CD20モノクローナル抗体「リツキサン®」
―視神経脊髄炎スペクトラム障害(視神経脊髄炎を含む)の再発予防に対する承認取得について―
日本医療研究開発機構の難治性疾患実用化研究事業として、宇多野病院 臨床研究部で実施された治療薬開発研究(研究代表者 田原将行)について、下記の通りプレスリリースがございましたのでご報告いたします。
今回の承認は、日本医療研究開発機構研究費による支援の下に、独立行政法人 国立病院機構宇多野病院臨床研究部 田原将行 医長、大江田知子 臨床研究部長、澤田秀幸 副院長を中心として国内の8施設で実施された、日本人視神経脊髄炎または視神経脊髄炎スペクトラム障害患者に対するリツキサンの再発抑制効果を検証した医師主導の第II/III相臨床試験(RIN-1試験)の結果に基づいています。
各社プレスリリース
全薬工業:https://www.chugai-pharm.co.jp/news/detail/20220620170000_1226.html
中外製薬株式会社:https://www.zenyaku.co.jp/iyaku/doctor/index.html
研究概要
背景
視神経脊髄炎(以下、NMO)は、我が国で昭和47年から取り組まれてきた特定疾患の一つ、多発性硬化症(以下、MS)に含まれていました。MSとNMOの2つの疾患は、視神経炎や脊髄炎といった類似の症状を示すため、明確に分けることが困難とされてきましたが、2005年にNMO患者にのみ検出される自己抗体(抗AQP4抗体)が発見されたことで、2つの疾患の病態解明が進み、2015年の難病法施行後は、多発性硬化症/視神経脊髄炎(特定疾患13)と2つの疾患名が併記して扱われています。NMOでは様々な症状を呈することがあることから、最近ではNMOという病名よりは、むしろNMOスペクトラム障害(以下、NMOSD)と呼ばれるようになっています。
MSに対する再発予防治療薬は、NMOに対しては有効でないことが判明しました。ステロイド薬はNMOの再発予防に有効であるものの、多くの副作用を伴うため、NMOのための再発予防治療薬の開発が急務でした。
体の様々な部位に作用するステロイド薬とは異なり、リツキシマブは、抗CD20モノクローナル抗体であり、免疫細胞の一つである血液中のB細胞のみに作用する分子標的薬です。そのため、ステロイド薬投与時に問題となる糖尿病や脂質異常症、ムーンフェイスやニキビといった美容的問題、骨粗鬆症、白内障や緑内障、大腿骨頭壊死といった副作用の心配は、リツキシマブではありません。リツキシマブはこうした副作用がなく、十分な免疫抑制効果を持つことから、NMOの再発抑制にも応用可能であると期待されました。そこで、宇多野病院臨床研究部では、リツキシマブの効果・安全性を検討するべく医師主導治験(RIN-1試験)を計画しました。公的研究費のサポートの下、治験のデザイン、プロトコールも宇多野病院臨床研究部内で独自に検討作成されたものです。治験では、抗AQP4抗体陽性、ステロイド内服中(プレドニゾロン換算5-30mg/日)、EDSS(注1)7点以下の16~80歳までのNMO患者を対象として、ステロイドの緩徐な減少を行いながら、治験薬を半年ごとに投与しました。4週毎に神経学的診察(EDSS、QOSI(注2))を実施し、眼科診察やMRI検査等を定期的に実施し、72週間の観察を行いました。
結果

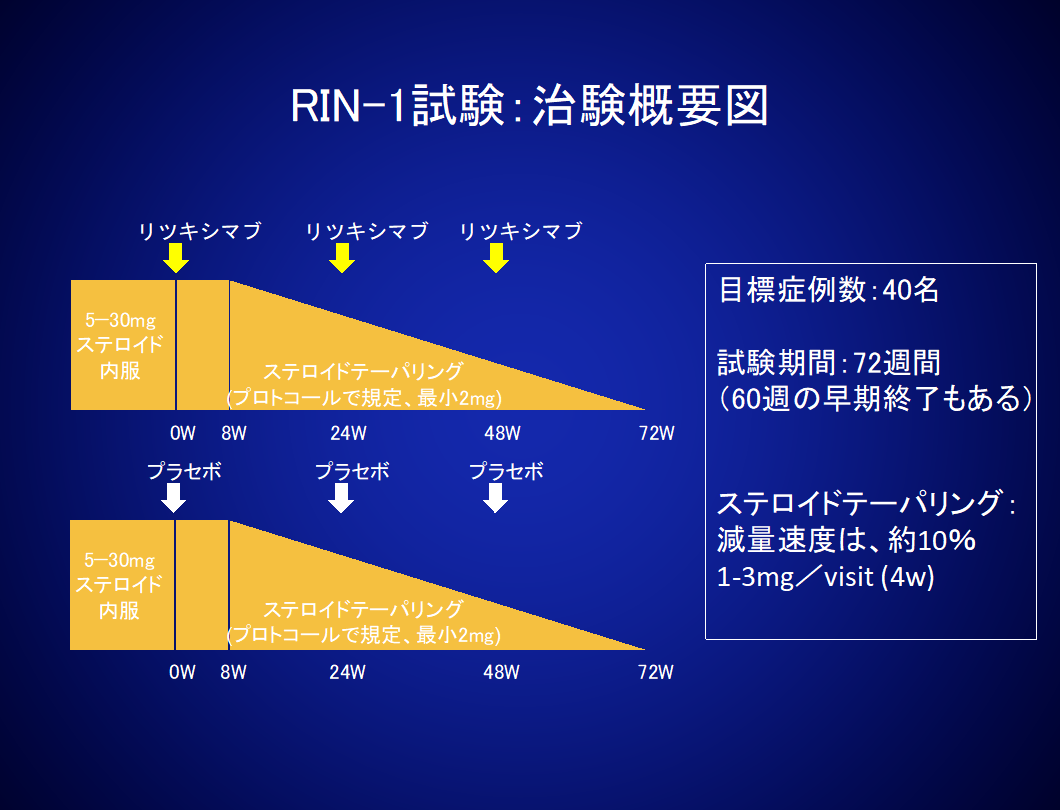
2014年5月から2017年8月までに、全国8施設でNMOの患者さんの協力をお願いしました。総数は42名(内、4名は治験の条件を満たさず除外)にご同意いただき、38名の患者さんがランダムに実薬(リツキシマブ)投与またはプラセボ(リツキシマブと外観は区別つかないが薬としての作用がないもの)投与に19名ずつ割り付けられました。治験は2019年1月に終了し、リツキシマブ群で3名の脱落(同意撤回などの理由で治験の途中で治験参加を中止すること)がありました。
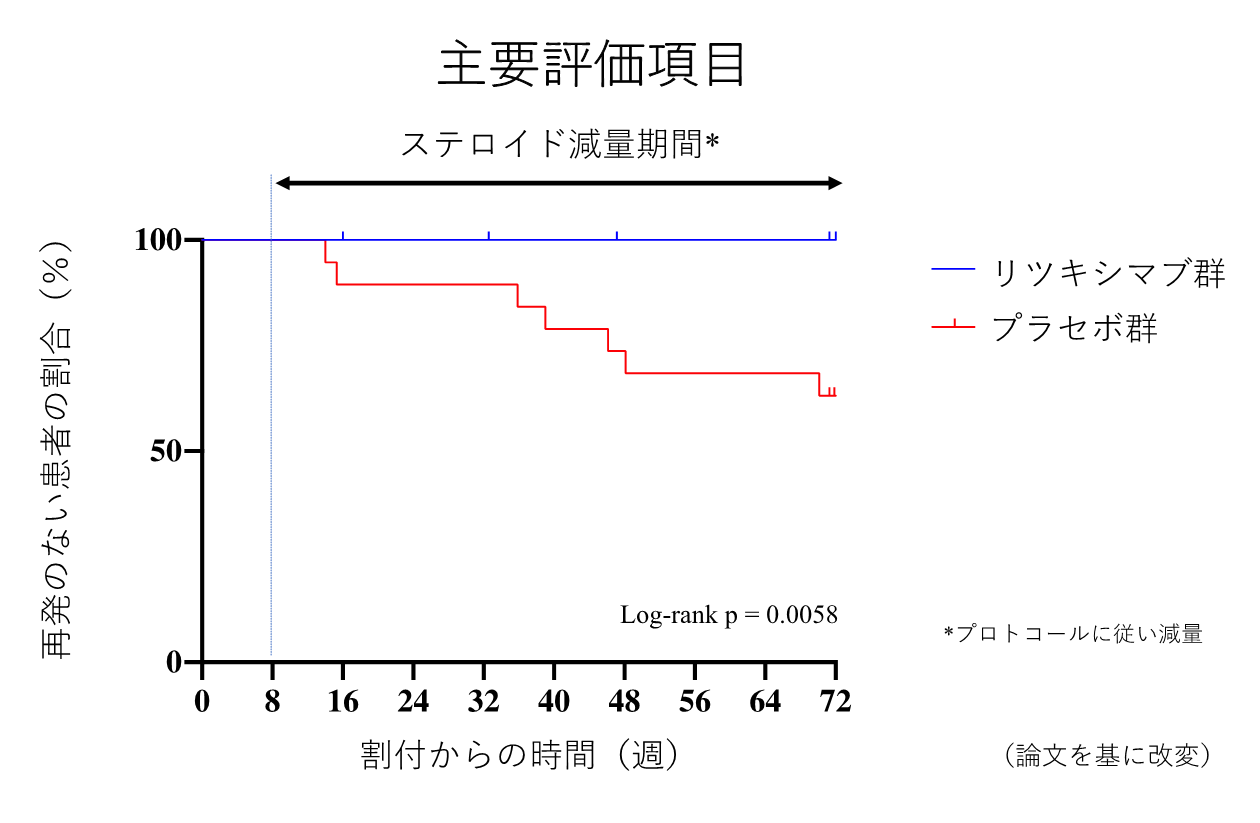
治験期間中にプラセボ群で7件の再発が認められましたが、リツキシマブ群で再発は一件も認められませんでした。主要評価項目である初回再発までの時間による生存分析では、有意差(Log-rankテスト;p = 0.0058)が示されました。副次評価項目であるEDSS変化量は、プラセボ群で-0.26、リツキシマブ群で-0.32と有意差はありませんでしたが、QOSI変化量は、プラセボ群0.63と比較し、リツキシマブ群-1.16と有意に(p = 0.0331)低下していました。ステロイド減量率は、プラセボ群で65.3%、リツキシマブ群で75.1%と有意差はみられませんでした。
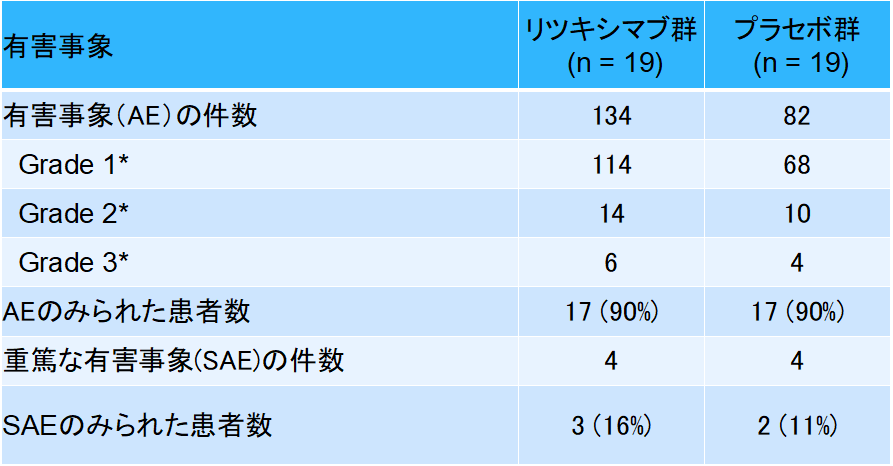
*「医薬品等の副作用の重症度分類基準について(平成4年6月29日薬安第80号)」に基づく
有害事象は、リツキシマブ群で134件、プラセボ群で82件報告されたものの主にGrade1-2であり、重篤な有害事象は8件でいずれも回復しており死亡例はありませんでした。
まとめ
本研究により、リツキシマブが抗アクアポリン4抗体陽性のNMOSDスペクトラム障害の患者さんの再発予防に有効な治療薬であることが示されました。以上の結果は、臨床神経学のトップ国際誌の一つであるランセット・ニューロロジー誌(The Lancet neurology)に掲載されました。
論文情報
掲載誌
The Lancet neurology
タイトル
Safety and efficacy of rituximab in neuromyelitis optica spectrum disorders (RIN-1 study): a multicentre, randomised, double-blind, placebo-controlled trial.
著者名
Tahara M, Oeda T, Okada K, Kiriyama T, Ochi K, Maruyama H, Fukaura H, Nomura K, Shimizu Y, Mori M, Nakashima I, Misu T, Umemura A, Yamamoto K, Sawada H.
DOI
10.1016/S1474-4422(20)30066-1.
本研究への支援
本研究は、下記機関より支援を受けて実施されました。
- 日本医療研究開発機構(AMED)難治性疾患実用化研究事業
研究課題「視神経脊髄炎の再発に対するリツキシマブの有用性を検証する第2/3相 多施設共同プラセボ対照無作為化試験」(主任研究者 田原将行;2015~2017年度) - 厚生労働科学研究費補助金 難治性疾患等実用化研究事業(難治性疾患実用化研究事業)
「視神経脊髄炎の再発に対するリツキシマブの有用性を検証する第2/3相 多施設共同プラセボ対照無作為化試験」(研究代表者 田原将行)(平成26年度) - 厚生労働科学研究費補助金 難治性疾患等克服研究事業(難治性疾患克服研究事業)
「視神経脊髄炎の再発に対するリツキシマブの有用性を検証する第2/3相 多施設共同プラセボ対照無作為化試験」(研究代表者 田原将行)(平成25年度) - 全薬工業株式会社(2014~2018年度:治験薬提供、2019年度~:研究費助成)
- 厚生労働科学研究費補助金 難治性疾患政策研究事業
研究課題「神経免疫疾患のエビデンスによる診断基準・重症度分類・ガイドラインの妥当性と患者QOLの検証」(主任研究者 松井真;2017~2019年度)
用語説明
(注1)EDSS
多発性硬化症で用いられる神経学的な評価尺度。0点から10点(高いほど悪い)。例えば、歩行が難しく、車椅子を使用していれば7点となる。
患者の状態を評価するために、視神経脊髄炎の患者にも使われている。
(注2)QOSI
視神経脊髄炎の評価のために開発されたスケール。0点から69点(高いほど悪い)
お問い合わせ先
研究成果(治験)に関する問い合わせ先
国立病院機構宇多野病院管理課
TEL:075-461-5121
e-mail: 405-utano@mail.hosp.go.jp