診断のための検査
診断のための検査
パーキンソン病やレビー小体病の診断には病気の経過、診察所見に加え、MRIやMIBG検査などが参考になります。
パーキンソン病では脳内のドーパミン神経細胞数が減少していますが、これをMRIで確認することはできません。つまり、パーキンソン病患者さんの脳MRIは基本的には異常が見られません。一方、多系統萎縮症や進行性核上性麻痺の患者さんでは脳MRIで特徴的な所見が見られることが多いので、診断に重要な所見となります。
また、心筋MIBGシンチグラムは、心臓の筋肉内のノルエピネフリン神経の密度を調べる検査です。最近の研究によって、心臓のノルエピネフリン神経がパーキンソン病やレビー小体病の患者さんの大部分で減少することがわかってきました。したがって、これを調べることにより、より正確な診断が可能になります。
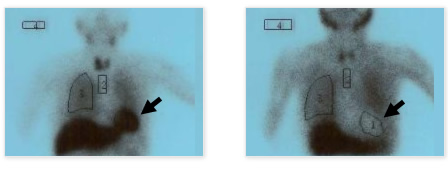
正常な場合は、検査では左の写真のように心臓の部分が黒く見えます(矢印)。一方、心臓の交感神経が減少していると右の写真のように心臓の部分は黒く見えません(矢印)。この検査は、内服薬の影響や心臓の機能の影響受けますので、これらを加味して結果を判断する必要があります。このほかにも種々の検査が診断に有用です。詳細は担当医にお尋ねください。
血中レボドパ濃度測定検査
当院では、パーキンソン病患者さんの治療について、とてもきめ細やかな対応を心がけています。
その取り組みの一つに、血中レボドパ濃度測定検査があります。
パーキンソン病患者さんの中には、病気が進行するにつれて、抗パーキンソン病薬の効き目が乏しくなったり、効いている時間が短くなったりすることがあります。その結果、1日の中で、パーキンソン病症状が強くなり、動きにくくなる時間帯(オフ時間)が出現することが知られています。
これには、抗パーキンソン病薬を内服するタイミングや量を適切に調節することで、オフ時間が短くなり、1日の症状が改善することが十分に期待できます。
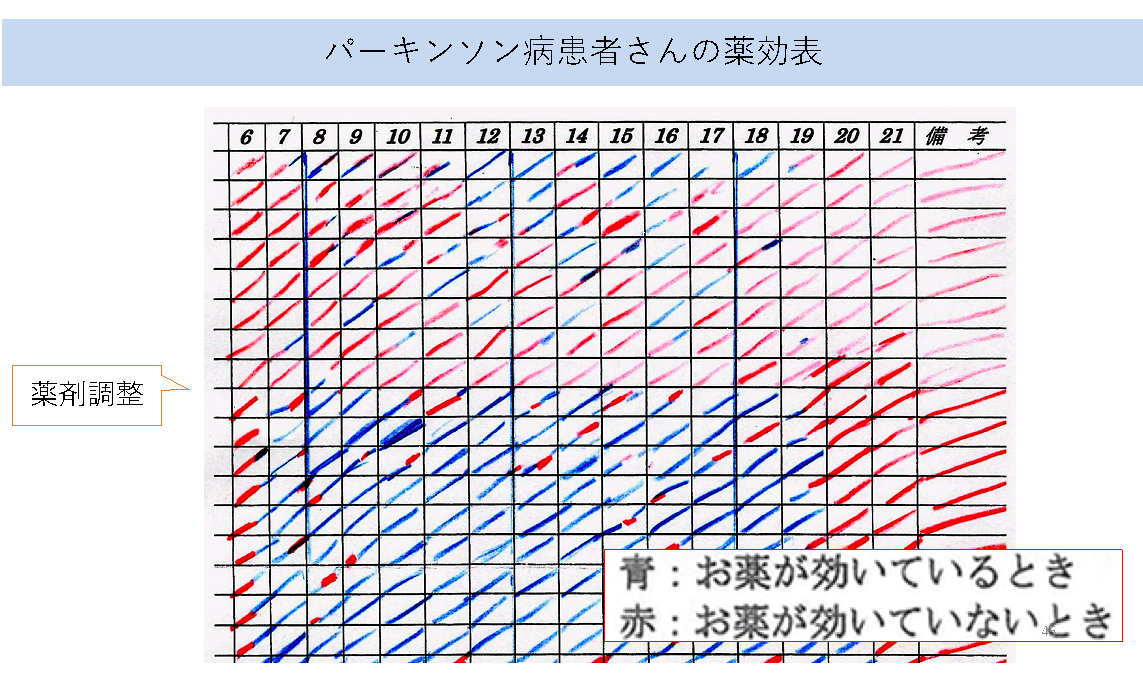
パーキンソン症状が1日の中で大きく変動したり、お薬の効果が乏しい時間帯(オフ時間)が問題になる場合には、まずは外来診療中に担当医師が問診したり、薬効表(図1)を実際に患者さんに記載していただくことで、薬の内服時間とオフ時間がどのように関係しているかを明らかにします。抗パーキンソン病薬をできるだけ適正に脳に届けることができるように、お薬の時間と量を調整します。
しかしながら、外来での薬の調整を行ってもオフ時間が残ってしまったり、抗パーキンソン病薬による副作用(ジスキネジア、幻覚、妄想など)が出ている場合には、血中レボドパ濃度測定検査の結果をもとに薬調整を行うと、病状が大きく改善することがあります。
実績
血中レボドパ濃度測定検査件数(のべ)
| 2016年 | 2017年 | 2018年 | 2019年 | 2020年 | 2021年 |
|---|---|---|---|---|---|
| 24件 | 36件 | 48件 | 44件 | 65件 | 76件 |
以下に実際の患者さんの経過例を提示します。
78歳男性
主訴
レボドパの効き目が切れてしまい、動けなくなる
経過
| 71歳 | 歩きにくさが出現しました。 |
|---|---|
| 74歳 | 当科を受診し、パーキンソン病と診断されました。 当初は、ドパミンアゴニストとレボドパの併用(ペルゴリド750μg、レボドパ・カルビドパ配合剤100mg×3回/日)により、終日、動作や歩行に問題なく過ごすことができました。 |
| 75歳 | レボドパの薬効の持続時間が短くなり、昼食前および夕方になるとパーキンソン症状の悪化(ウェアリング・オフ現象)がみられたため、レボドパを1日5回に分けて服用するようになりました。 |
| 76歳 | 薬効がみられている時間(オン時間)に一致して、体幹が左右に大きく揺れるような不随意運動(ジスキネジア)が出現するようになりました。また、オフ時間になると「身体全体がだるい」、「頭がくらくらして顔がほてる」、「おなかが痛い」などの訴えが出現するようになりました。頓用のレボドパ・カルビドパ配合剤(100mg)を追加服用すると、それらの症状はおさまりました。 |
| 78歳 | オフ時間が増えるとともに、オフ時の動作や歩行の悪化がみられるようになりました。その一方で、オン時のジスキネジアが強くなったので、薬の調整目的に入院となりました。 |
問題点
(1) ウェアリング・オフ現象(薬効の持続時間が短くなり症状が悪化する現象)
(2) ジスキネジア(オン時に出現する不随意運動)
(3) 非運動症状(オフ時間に出現する腹痛)
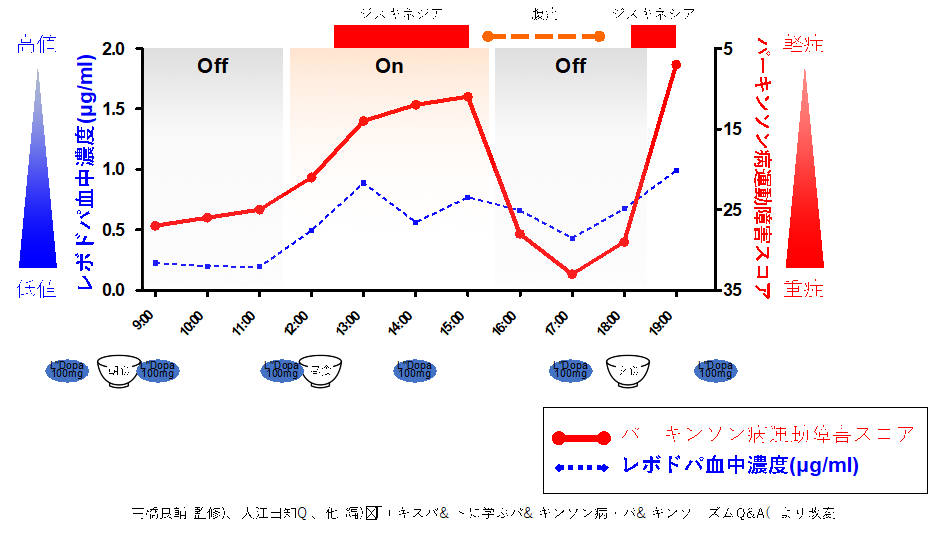
薬の調整を行うにあたり、まずはパーキンソン症状の日内変動と血中レボドパ濃度測定検査を行いました(図2)。
パーキンソン病にともなう運動症状については、12~15時、および19時はオン時間と考えられましたが、9~11時、および16~18時はオフ時間と考えられました。一方で、血中レボドパ濃度を観察すると、午前中はレボドパ服用後も血中濃度が上昇せず、13時に血中濃度のピークが遅れてみられました。その後、17時に血中濃度の低下があり、19時に再びピークがみられました。運動症状のスコアは、レボドパ血中濃度の推移とおおむね一致していました。ジスキネジアの出現時間はオン時間に一致していました。
血中レボドパ濃度測定検査から明らかになった問題点と対策
(1) 午前中の血中濃度の立ち上がりが遅く、レボドパの効果発現に時間を要するdelayed on(=内服後すぐに薬効が発現しないこと)が観察されました。パーキンソン病により胃の蠕動運動が低下し、胃内容物が輸送されるのに時間を要するために、朝食後に服用したレボドパの吸収が遅れていることが示唆されました。
対策 → 朝食後のL-ドパ服用を朝食前に変更
(2) レボドパの血中濃度が維持されず、16~18時にウェアリング・オフが観察されました。脳内のドパミン神経終末の減少にともなう脳内ドパミン保持能の低下が示唆されました。
対策 →レボドパ血中濃度が維持されるように、末梢性COMT阻害薬を追加
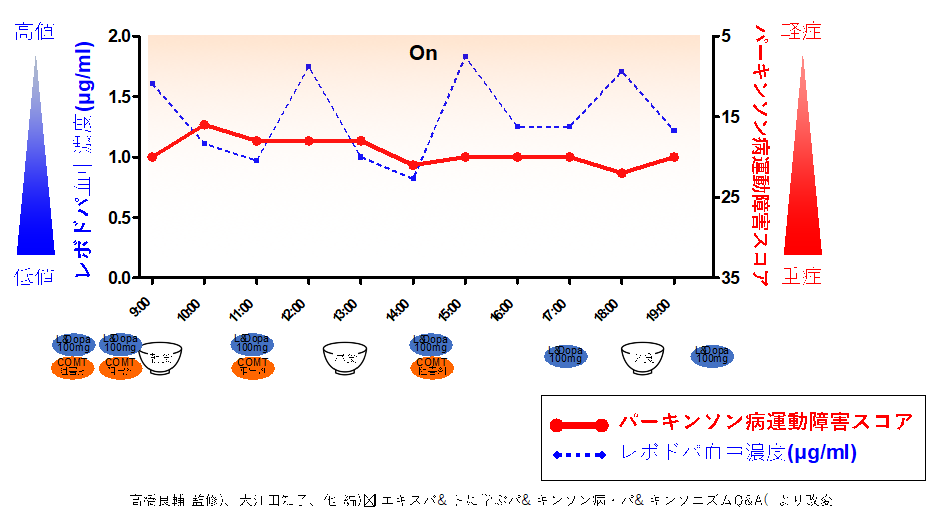
薬剤調整後に、血中レボドパ濃度測定検査を再び行いました(図3)。
その結果、オフ時間がなくなり、オフ時にみられた腹痛の症状も消失しました。また、日常生活動作を障害するような強いジスキネジアもみられなくなりました。血中レボドパ濃度を観察すると、入院時の検査で午前中および夕方にみられた血中レボドパ濃度の低下はなくなり、1.0~2.0μg/mLのあいだに維持されていました。症状が改善したため、退院となりました。